Il campo della ricerca sul cancro alla prostata sta diventando sempre più attratto dalla potenziale utilità clinica della glicoproteina transmembrana FOLH1 (nota anche come antigene della membrana specifico della prostata, PSMA). La specificità relativa di questa molecola come un ligando di superficie della cellula prostatica del cancro [1] e il suo ruolo emergente nella tomografia a emissione di positroni (PET) e nella terapia diretta dalle cellule [2] sono nuovi interessanti sviluppi con un potenziale illimitato. Questa eccitazione è giustificata? La scansione PSMA-PET sta iniziando a fornire [[3], [4]] e attendiamo con impazienza protocolli e linee guida per ottimizzare l’utilizzo di questo romanzo, modalità di messa in scena apparentemente delicata nel processo decisionale prima e dopo il trattamento radicale.
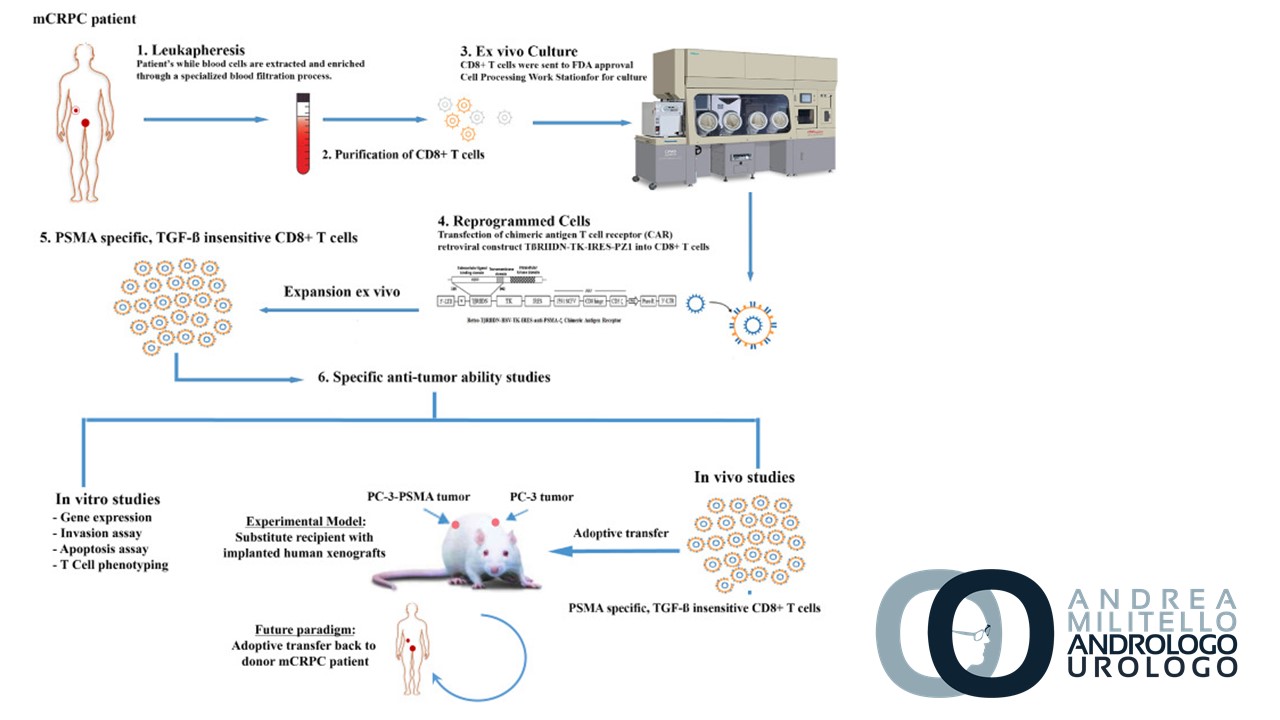 Mentre i ricercatori hanno iniziato a considerare il potenziale della PSMA nella terapia mirata, le prove rimangono scarse fino ad oggi. In questo numero di Urologia europea, Zhang et al [5] presentano interessanti nuovi dati utilizzando cellule T CD8 + ricombinanti prelevate da un paziente con carcinoma prostatico e modificate per bersagliare le cellule che esprimono PSMA per resistere all’ospite TGF-β. Queste cellule immunitarie modificate sono state utilizzate per inibire cellule PC-3 esprimenti PSMA trasformate, un modello di linea cellulare umana derivato da una metastasi ossea della prostata, in esperimenti sia in vitro che in vivo. Gli autori propongono un mezzo per modificare la risposta immunitaria dell’ospite a cellule bersaglio di cancro alla prostata che esprimono un ligando specifico della superficie cellulare (in questo caso PSMA).
Mentre i ricercatori hanno iniziato a considerare il potenziale della PSMA nella terapia mirata, le prove rimangono scarse fino ad oggi. In questo numero di Urologia europea, Zhang et al [5] presentano interessanti nuovi dati utilizzando cellule T CD8 + ricombinanti prelevate da un paziente con carcinoma prostatico e modificate per bersagliare le cellule che esprimono PSMA per resistere all’ospite TGF-β. Queste cellule immunitarie modificate sono state utilizzate per inibire cellule PC-3 esprimenti PSMA trasformate, un modello di linea cellulare umana derivato da una metastasi ossea della prostata, in esperimenti sia in vitro che in vivo. Gli autori propongono un mezzo per modificare la risposta immunitaria dell’ospite a cellule bersaglio di cancro alla prostata che esprimono un ligando specifico della superficie cellulare (in questo caso PSMA).
Questo nuovo uso di PSMA nell’immunoterapia diretta dalle cellule apre una strada intrigante e promettente di terapia per i pazienti, con applicazioni nella storia naturale del cancro alla prostata. Per quanto a nostra conoscenza, questo è il primo rapporto sull’immunoterapia mirata al PSMA. Si basa su precedenti descrizioni dell’impiego dell’immunoterapia nel carcinoma della prostata, che ad oggi è essenzialmente limitato a Sipuleucel T [6], la prima immunoterapia approvata dalla Food and Drug Administration (FDA) negli Stati Uniti per qualsiasi tipo di cancro dell’organo solido, sebbene il suo utilizzo è stato limitato nella pratica clinica. Nel 2017 la FDA ha raccomandato CTL109, una terapia con cellule T del recettore dell’antigene chimerico, come trattamento per la leucemia linfoblastica acuta pediatrica (ALL), aprendo la strada a una generazione di terapie a cellule T ricombinanti nella leucemia. Ma che dire dei tumori di organi solidi come il cancro alla prostata?
Dati genetici molecolari suggeriscono che tutti gli individui hanno cellule con cambiamenti maligni, sia che si trovino nell’ambiente circolante o all’interno di organi solidi. Perché queste cellule mutate non formano tumori più frequentemente? La risposta a questa domanda è quasi certamente perché abbiamo un sistema immunitario funzionante, che si traduce in una frequente eliminazione delle cellule cancerogene "canaglia" in un processo noto come immunoediting [[7], [8]]. In assenza di un sistema immunitario competente, i tumori hanno maggiori probabilità di svilupparsi. Un classico esempio è lo sviluppo del sarcoma di Kaposi in pazienti sieroconversi immunocompromessi con virus dell’immunodeficienza umana [9]. Inoltre, è ora chiaro che esiste una logica intrinseca per imbrigliare il sistema immunitario al fine di distruggere le cellule tumorali, in quanto questo è uno dei meccanismi naturali di lotta contro il cancro del corpo [8].
Il termine recettore dell’antigene chimerico si riferisce al processo mediante il quale una cellula figlia viene prodotta con un genotipo alterato (chimera), dirigendo il complesso di riconoscimento dell’antigene su un bersaglio molecolare specifico come PSMA (o il recettore CD19 nel caso della terapia ALL descritta sopra).
Si ritiene che molteplici meccanismi inibitori impediscano l’eliminazione immuno-mediata delle cellule tumorali della prostata, comprese le cellule T regolatorie, i macrofagi associati ai tumori, le cellule soppressorie derivate da mieloidi e le molecole inibitrici [[10], [11]]. Poiché il carcinoma della prostata ha un pattern di mutazione somatica limitata [[12], [13]] e un carico di antigene associato al tumore [14], si ritiene che questa neoplasia non sia suscettibile all’immunoterapia come altri tumori di organi solidi con una maggiore immunogenicità carico, come i tumori del polmone e della vescica. Tuttavia, l’immunogenicità del cancro alla prostata in potenziale immunoterapia è stata dimostrata da studi iniziali che combinavano trattamenti convenzionali con modulatori del checkpoint immunitario come gli anticorpi monoclonali anti-PD-1 / anti-PD-L1 / anti-CTLA4 [15]. Pertanto è del tutto plausibile che un’immunoterapia diretta con PSMA come quella descritta da Zhang et al possa produrre benefici clinici per i pazienti con cancro alla prostata.
Mentre la capacità di modificare le cellule immunitarie per colpire le cellule che esprimono PSMA ha dato risultati impressionanti nei modelli preclinici, non è ancora chiaro se questo sarà l’approccio ottimale e l’obiettivo ideale in un contesto clinico. Ulteriori prove sono necessarie dall’imaging per dimostrare che il PET basato su PSMA rileva in modo affidabile una malattia metastatica di piccolo volume. Come prova di principio, Zhang e altri offrono un modello per la terapia immunitaria mirata basata sul ligando e, in definitiva, per un ciclo traslazionale dal paziente al laboratorio al paziente. La validazione richiederà, ovviamente, ulteriori modelli preclinici derivati ​​dal paziente prima che la tecnologia sia pronta per le applicazioni cliniche. Tuttavia, nell’attuale rapido ritmo di progresso, bisogna essere ottimisti sul fatto che ciò sarà realizzato nei prossimi anni.
L’utilizzo futuro della molecola di superficie cellulare quasi-onnipresente PSMA promette molto nella gestione del cancro alla prostata e questo studio rivela un’altra strada eccitante per sfruttare questo ligando. Inoltre, l’eradicazione delle cellule tumorali mediata da cellule T detiene un potenziale significativo per la pratica clinica futura [16]. Rimangono diverse domande. A che punto della storia naturale di questa malattia relativamente indolente prevediamo l’attuazione dell’immunoterapia? Possono essere usati altri ligandi specifici per il cancro alla prostata al posto di PSMA? Quali altri aspetti dell’immunità innata e acquisita potrebbero essere rafforzati per sradicare la malattia micrometastatica disseminata? E quale proporzione di uomini con carcinoma della prostata ospita cellule letali circolanti di cancro alla prostata? Ci sono poche risposte fino ad oggi, ma opportunità senza precedenti per una nuova ricerca pionieristica.
