Curioso della terapia con peptidi Frag 176-191? All’interno descrivo in dettaglio tutto ciò che devi sapere sulla sostanza chimica di ricerca: dosaggio, benefici, effetti collaterali e altro ancora.
Questa guida approfondita sulla terapia del peptide Frag 176-191 è stata realizzata dal team di ricerca di Peptides.org, la principale fonte per tutte le informazioni sui peptidi di ricerca, SARM e altro ancora.

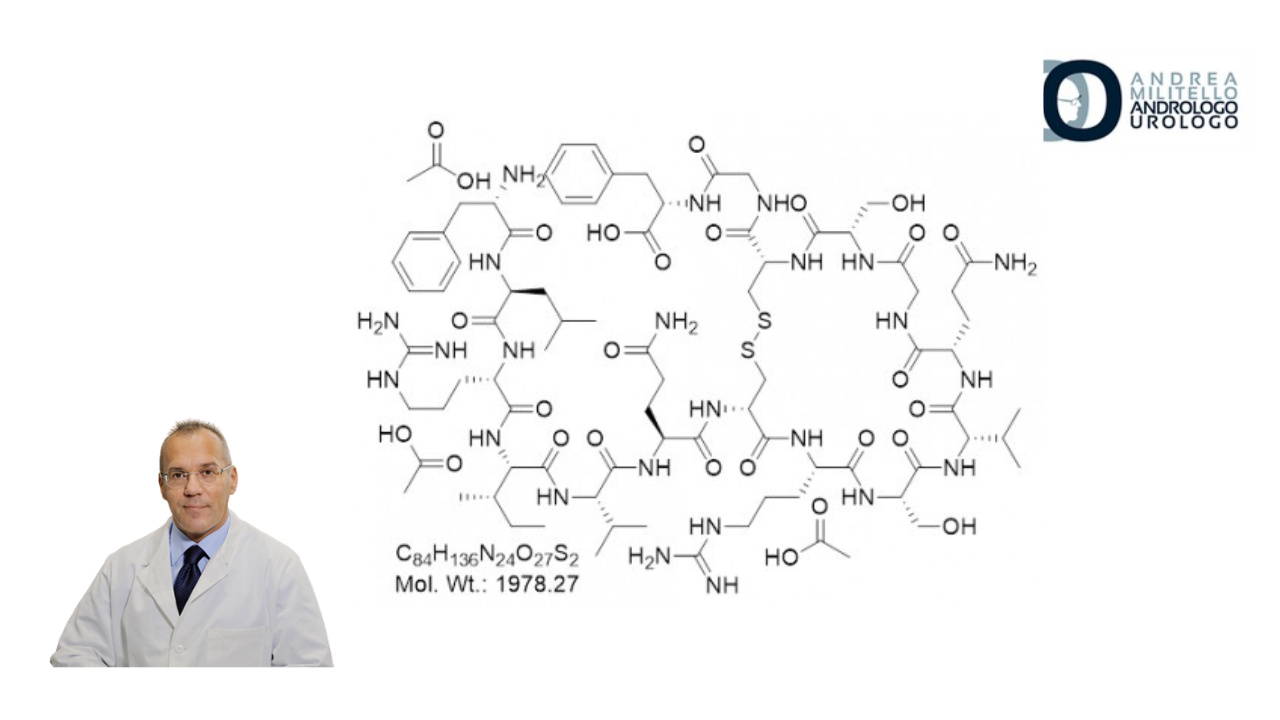
Il frammento dell’ormone della crescita umano 176-191 – noto anche come frag 176-191 – è un peptide sintetico identico ai 16 amminoacidi finali dell’ormone della crescita umano (hGH). Di conseguenza, questo frammento conserva un sottoinsieme degli effetti consolidati di hGH sulla perdita di grasso, senza gli effetti indesiderati aggiuntivi legati alla proteina hGH completa.
Sulla base della scoperta che un piccolo frammento della proteina hGH può guidare selettivamente la perdita di grasso senza i rischi associati all’aumento dei livelli di IGF-1, una notevole quantità di ricerca e sviluppo è stata dedicata ai peptidi sintetici che imitano l’attività di questo piccolo frammento di hGH.
Un altro frammento di hGH denominato AOD9604 ha ricevuto la massima attenzione ed è quasi identico al frammento 176-191, poiché entrambi i peptidi condividono la stessa sequenza di aminoacidi dalle posizioni 177 a 191. Dato l’elevato grado di somiglianza, molti esperti considerano l’ampia ricerca clinica eseguita per AOD9604 per essere rilevante per frag 176-191.
In questo articolo, si fornisce una panoramica completa della ricerca pertinente associata a frag 176-191, nonché linee guida di riferimento per il dosaggio e la somministrazione.
Cos’è il Frag 176-191?
Il frammento 176-191 dell’ormone della crescita umana (frag 176-191) è stato scoperto dal dottor Frank Ng negli anni ’90 presso l’Università di Monash ed è responsabile degli effetti brucia grassi della proteina completa dell’ormone della crescita umana (hGH) [1, 2].
Similmente al peptide derivato AOD9604, che verrà spiegato in seguito, diversi studi precedenti hanno utilizzato un peptide quasi identico chiamato frag 177-191 (noto anche come AOD9601). Date le similitudini di sequenza e sovrapposizione nella legame ai recettori, la letteratura su questi peptidi derivati è rilevante per la considerazione del frag 176-191 e verrà utilizzata in modo interscambiabile in questo articolo.
La proteina progenitrice del frag 176-191, l’hGH, è una proteina composta da 191 aminoacidi che regola una complessa interazione di diversi processi fisiologici, dalla crescita cellulare e tissutale alla perdita di grasso e al metabolismo del glucosio [3].
Analogamente a molte altre proteine multifunzionali, diversi processi sono controllati da diverse regioni della proteina hGH [4]. Ad esempio, circa i primi 45 aminoacidi sono responsabili della promozione della sintesi dell’insulina, mentre gli ultimi 16 aminoacidi sono responsabili della perdita di grasso [5].
Grazie alla natura modulare dell’hGH, è possibile utilizzare specifici frammenti della proteina per controllare selettivamente le funzioni associate a quella parte specifica della proteina.
Di conseguenza, la scoperta che gli ultimi 16 aminoacidi conferiscono gli effetti brucia grassi dell’hGH ha portato i ricercatori a sintetizzare separatamente il frag 176-191 come un peptide autonomo. Come previsto, il frag 176-191 è in grado di indurre la perdita di grasso senza gli altri effetti associati alla proteina completa dell’hGH [6].
A causa della gravità dell’epidemia di obesità, questa scoperta è stata una pietra miliare, poiché i medici si trovano ancora ad affrontare un insieme molto limitato di strumenti farmacologici per aiutare i pazienti a perdere peso, dato che l’utilizzo della proteina completa dell’hGH provoca troppi effetti collaterali per un uso a lungo termine.
Nel tentativo di migliorare la stabilità del peptide, i ricercatori hanno modificato il primo aminoacido nel peptide frag 176-191 da a-fenilalanina a a-tirosina, ottenendo così un nuovo peptide chiamato anti-obesity drug 9604, o AOD9604 [5, 7].
AOD9604 è il frammento dell’hGH lipolitico più ampiamente studiato fino ad oggi ed è stato valutato in sei studi clinici [5]. Grazie alla quasi identica similitudine di sequenza e, cosa più importante, alla conservazione al 100% della regione del peptide necessaria per indurre la lipolisi, molti ricercatori considerano la letteratura su AOD9604 rilevante anche per il frag 176-191 [8].
Qual è il ruolo di Frag 176-191?
Nonostante il meccanismo d’azione preciso non sia chiaro, si ritiene che il peptide frag 176-191 mimi l’attività lipolitica dell’hGH lasciando invece inalterati gli altri processi normalmente influenzati dall’hGH [7, 8]. Per comprendere meglio come funziona il frag 176-191, è necessario capire la funzione della proteina progenitrice, l’hGH.
L’hGH è una proteina composta da 191 aminoacidi che influenza una serie complessa di processi fisiologici, con azioni anaboliche e cataboliche su diversi tessuti del corpo [3, 4, 9]. Ad esempio, l’hGH ha un ruolo causale nella crescita durante la pubertà e può causare iperplasia dei tessuti adulti in disturbi come l’acromegalia, ma svolge anche un ruolo importante nella promozione della perdita di grasso [10, 11, 12].
La natura funzionale diversificata dell’hGH è correlata alla sua struttura di dominio proteico multifunzionale, con diversi domini proteici responsabili di diverse azioni biochimiche [13].
Per questo motivo, il frag 176-191 è in grado di indurre selettivamente la perdita di grasso in modo simile all’hGH, ma senza gli effetti indesiderati aggiuntivi come la crescita dei tessuti, l’ipertensione e l’edema [5, 14].
Il profilo di attività selettiva del frag 176-191 rispetto all’hGH, largamente informato dalla letteratura su AOD9604, è reso possibile dal fatto che il 176-191 non può legarsi al recettore dell’ormone della crescita [7, 15]. Di conseguenza, tutti i processi che dipendono dalla segnalazione del recettore dell’ormone della crescita, compresa l’upregulation della produzione di IGF-1, non sono influenzati dal peptide frag 176-191.
Sebbene le interazioni molecolari che mediano gli effetti di perdita di grasso del frag 176-191 siano sconosciute, si sa che l’hGH induce la perdita di grasso aumentando i livelli circolanti di acidi grassi liberi (FFA) mediante l’aumento della lipolisi e l’inibizione dell’assorbimento di FFA nelle cellule adipose [4, 9].
Infine, ci sono evidenze che il frag 176-191 possa influenzare positivamente la rigenerazione della cartilagine attraverso un meccanismo simile a quello dell’hGH, ancora una volta senza gli effetti negativi sul metabolismo del glucosio [16].
Studi clinici e ricerca su Frag 176-191
Non sono stati condotti studi clinici utilizzando il frammento 176-191 dell’ormone della crescita umana (frag 176-191), poiché i ricercatori hanno invece scelto di utilizzare il peptide derivato quasi identico, AOD9604 [5].

Come descritto in precedenza, la letteratura su AOD9604 è considerata dagli esperti rilevante per comprendere la biologia del frag 176-191 e verrà citata in questa sezione.
Studi preclinici su animali
In ratti Zucker obesi a cui è stata somministrata una dose orale giornaliera di 500 mcg di AOD9604, si è osservato una significativa riduzione dell’aumento di peso corporeo rispetto ai controlli [17]. È importante notare che i topi trattati per via orale non hanno perso peso, ma hanno guadagnato peso ad un ritmo più lento rispetto ai controlli.
È interessante notare che negli studi precedenti, i topi trattati con AOD9604 iniettabile hanno effettivamente perso peso rispetto al punto di partenza, il che rappresenterà una distinzione rilevante nella discussione degli studi clinici sull’uomo [18].
Per comprendere il meccanismo d’azione del frammento lipolitico dell’hGH, i ricercatori hanno utilizzato topi geneticamente modificati privi del recettore adrenergico beta-3 (β3-AR) per capire se gli effetti lipolitici di AOD9604 sono mediati da β3-AR [7].
Interessantemente, gli autori dello studio hanno scoperto che sia l’hGH che il suo frammento lipolitico in parte esercitano i loro effetti lipolitici modulando l’espressione del recettore β3-AR. Tuttavia, si è osservato che i topi privi di β3-AR rispondono acutamente ad AOD9604, dimostrando che esiste un effetto lipolitico indipendente da β3-AR di AOD9604.
Infine, uno studio su conigli ha evidenziato che AOD9604 può promuovere la rigenerazione della cartilagine quando somministrato direttamente nell’articolazione del ginocchio, suggerendo un’altra promettente applicazione per il frammento di hGH [16].
Trials clinici sull’uomo
Sono stati condotti un totale di sei studi clinici sull’uomo tra il 2001 e il 2006 per valutare la sicurezza, la tollerabilità e l’efficacia di AOD9604 [5].
Nei primi due studi, la sicurezza di AOD9604 è stata valutata tramite infusione endovenosa (IV), che è unica rispetto alla maggior parte degli studi clinici su peptidi, che di solito vengono somministrati tramite iniezione sottocutanea o intramuscolare. In entrambi gli studi, AOD9604 è stato ben tollerato, senza osservare tendenze negli eventi avversi tra i gruppi di trattamento e di controllo [5].
È importante notare che non sono state osservate variazioni nei livelli di IGF-1, confermando l’ipotesi che il frammento lipolitico dell’hGH funzioni in modo indipendente dalle vie che promuovono la crescita dell’hGH [5]. Nonostante il profilo di sicurezza accettabile, i ricercatori hanno deciso di sviluppare una formulazione orale.
Sono stati condotti altri quattro studi clinici per valutare AOD9604 utilizzando una formulazione orale. Anche la somministrazione orale di AOD9604 è stata ben tollerata, raggiungendo il punto finale in ciascuno degli studi sulla sicurezza [5].
Tuttavia, gli studi clinici alla fine non hanno dimostrato che AOD9604 somministrato per via orale fosse efficace come farmaco anti-obesità, e gli studi clinici sono stati interrotti al termine di uno studio di fase IIb [5].
Alcuni esperti attribuiscono i risultati clinici deludenti alla decisione di sviluppare una formulazione orale, poiché la maggior parte dei peptidi ha una biodisponibilità minima quando assunti per via orale. Successivamente, AOD9604 è stato concesso in licenza a un’altra azienda farmaceutica che ha intrapreso un percorso di somministrazione diverso, riconoscendo i problemi legati alla somministrazione orale [19].

Sicurezza ed effetti collaterali di Frag 176-191
Come evidenziato in precedenza, i ricercatori non hanno condotto studi sull’uomo con il peptide frag 176-191, utilizzando invece il peptide quasi identico AOD9604 a causa di un ipotizzato aumento della stabilità. Di conseguenza, una valutazione della sicurezza di frag 176-191 deve essere extrapolata sulla base dei dati provenienti da AOD9604, che differisce solo per un amminoacido.
Attraverso sei studi clinici su AOD9604 che hanno coinvolto un totale di 893 soggetti, non sono stati riscontrati problemi di sicurezza attribuibili al peptide e AOD9604 ha mostrato un profilo di sicurezza eccellente [5]. È importante sottolineare che AOD9604 non ha causato nessuno degli effetti indesiderati del trattamento con hGH, compreso l’aumento di IGF-1 o il deterioramento del metabolismo del glucosio.
Nel primo studio clinico, 15 soggetti hanno ricevuto tre diverse dosi di AOD9604 (25mcg/kg a 400mcg/kg) e una dose di placebo, somministrati tramite iniezione endovenosa, separati da sette giorni. Nel corso dello studio, sono stati registrati un totale di 29 eventi avversi, sebbene le incidenze fossero tutte lievi e distribuite in modo uniforme tra il gruppo di trattamento e il gruppo di controllo, suggerendo l’assenza di un ruolo causale del peptide [5].
Un secondo studio su 23 soggetti che valutava una gamma di dosi più basse (25, 50 e 100mcg/kg) ha concluso con un insieme simile di conclusioni, poiché non c’era alcuna tendenza nell’incidenza degli eventi avversi tra il gruppo placebo e il gruppo di controllo e AOD9604 è stato ben tollerato. Tuttavia, in questo studio sono stati riscontrati tre eventi avversi considerati di intensità grave, di cui uno nel gruppo AOD9604 e due nel gruppo placebo. L’evento avverso nel gruppo AOD9604 (sensazione di oppressione al petto) è stato rilevante solo perché non è stato possibile escludere un legame con il trattamento con AOD9604 [5].
Nonostante il profilo di sicurezza complessivamente accettabile riscontrato in entrambi gli studi sulla sicurezza, lo sviluppo clinico si è spostato verso una formulazione orale di AOD9604. Nei restanti quattro studi clinici su AOD9604, non sono stati sollevati seri problemi di sicurezza. L’unico risultato degno di nota è stata l’aumentata frequenza di lievi effetti collaterali gastrointestinali osservati nel gruppo che ha ricevuto la dose più elevata (54mg) di AOD9604 per via orale [5].
Analogamente a AOD9604 somministrato per via endovenosa, non è stato osservato alcun aumento del livello sierico di IGF-1 quando AOD9604 è stato somministrato per via orale, né sono state riscontrate alterazioni del metabolismo del glucosio [5].
Note legali e doping negli States
Come altri peptidi di ricerca, il frag 176-191 è legale per l’acquisto, la vendita e la manipolazione solo a scopo di ricerca. Attualmente, il frag 176-191 non è disponibile come prodotto medico poiché non è approvato dalla FDA per nessun uso.
Di conseguenza, il frag 176-191 non può essere commercializzato negli Stati Uniti per il consumo umano né per il trattamento di condizioni mediche. Leggi simili si applicano nell’Unione Europea e nel Regno Unito.
La mancanza di regolamentazione per peptidi come il frag 176-191 ha portato a un mercato dei peptidi ampiamente non regolamentato, in cui venditori non qualificati promuovono inappropriatamente prodotti con affermazioni mediche non supportate. Questi venditori sono soggetti a sanzioni legali in molti paesi, inclusi gli Stati Uniti e il Regno Unito, mentre i consumatori sono esposti ai rischi derivanti dalla somministrazione di composti adulterati.
I ricercatori sono quindi invitati ad esercitare cautela e a assicurarsi di acquistare materiali da venditori qualificati con un lungo track record nella fornitura di peptidi di alta qualità per la ricerca.
Frag 176-191 per l’atletica competitiva
Per i ricercatori con l’intenzione di applicare il loro lavoro all’atletica competitiva, è importante notare che il frag 176-191 è classificato come sostanza vietata da diverse agenzie antidoping, a causa del suo potenziale per migliorare le prestazioni atletiche.
In particolare, il frag 176-191 è classificato come una sostanza S2 non specificata dall’Agenzia Mondiale Antidoping (WADA), che è stata adottata anche dall’Agenzia Antidoping degli Stati Uniti (USADA) [20, 21].
Dosaggio e ciclo di Frag 176-191
L’efficacia limitata del peptide del frammento 176-191 dell’ormone della crescita umana somministrato per via orale (frag 176-191) ha portato alla conclusione che il frag 176-191 dovrebbe essere somministrato preferibilmente tramite iniezione sottocutanea, simile all’hGH.
Dato che il peptide frag 176-191 è stato interrotto per la valutazione clinica, l’opinione degli esperti si è spostata verso un intervallo di dosaggio appropriato per la somministrazione sottocutanea di frag 176-191 di circa 200-500mcg al giorno, al fine di indurre la perdita di peso nei soggetti.
Nonostante AOD9604, l’equivalente di frag 176-191, abbia dimostrato un profilo di sicurezza eccellente, la tolleranza alle iniezioni sottocutanee dovrebbe comunque essere valutata inizialmente utilizzando dosi conservative [5].
Un protocollo ipotetico di dosaggio di Frag 176-191 per aiutare i ricercatori a comprendere la possibile progettazione dello studio è il seguente:
Dose iniziale: Per valutare la tolleranza, iniziare con una dose di frag 176-191 di 100mcg iniettata sottocutaneamente. Si tenga presente che 1mg equivale a 1000mcg e 100mcg equivale a 1/10 di milligrammo.
Dosi successive: Se la dose iniziale viene ben tollerata, aumentare la dose tra 200-500mcg per iniezione, a seconda degli obiettivi dello studio.
Tempistica e frequenza di somministrazione: Sulla base di quanto si sa sulla farmacocinetica e sulla farmacodinamica dell’hGH, il frag 176-191 è probabilmente meglio somministrato a stomaco vuoto, circa 30 minuti o 1 ora prima dell’esercizio. Si tenga presente che la dose giornaliera totale può essere suddivisa tra un’iniezione mattutina e serale.
Per le formulazioni intranasali di frag 176-191, la biodisponibilità sarà inferiore a causa della ridotta assorbimento della soluzione del peptide attraverso la membrana nasale, rispetto all’iniezione [22]. Per compensare la ridotta assorbimento sistemica, i ricercatori potrebbero considerare l’utilizzo del protocollo sopra elencato, ma con dosi aumentate ad ogni passaggio fino al 50%.
Frag 176-191 | Iniettabile vs Spray Nasale
Dalla scoperta di frag 176-191 e del suo derivato AOD9604, gli studi clinici hanno valutato la sicurezza e l’efficacia utilizzando sia l’iniezione che la somministrazione orale di pillole e capsule [5]. Date le scarsefficacia della somministrazione orale, nonché la lunga storia dell’uso dell’hGH iniettabile, la somministrazione di frag 176-191 tramite iniezione sottocutanea è la migliore opzione per massimizzare la biodisponibilità.
Un’altra via di somministrazione comunemente utilizzata per peptidi come il frag 176-191 è tramite spray nasale, che viene utilizzato in molte terapie peptidiche approvate dalla FDA e in studi clinici conformi alla FDA [23].
La membrana nasale è in grado di assorbire rapidamente peptidi e piccole proteine ed è stata oggetto di interesse da parte di ricercatori e aziende farmaceutiche che cercano di evitare le iniezioni, spesso meno desiderabili e che portano a una scarsa adesione del paziente [22]. Di conseguenza, è stato compiuto un notevole sforzo nello sviluppo clinico per validare la compatibilità dei peptidi e delle piccole proteine con l’amministrazione tramite spray nasale [23].
Per garantire che il peptide frag 176-191 venga somministrato con la massima biodisponibilità tramite spray nasale, i ricercatori possono tenere presente i seguenti fattori e linee guida quando si pensa a protocolli clinici ipotetici:
Per massimizzare l’assorbimento, lasciare almeno un minuto tra le spruzzate nella stessa narice per evitare una sovrabbondanza della membrana nasale e la conseguente perdita del peptide per via orale.
Somministrare ai soggetti con la testa inclinata per evitare perdite dalla parte inferiore del naso.
Eliminare eventuali congestioni nasali prima dell’amministrazione per ridurre al minimo l’ostruzione della membrana nasale e garantire un’assorbimento massimo.
Assicurarsi che l’erogatore dello spray sia mantenuto pulito e refrigerato quando non in uso per ridurre al minimo la contaminazione e la degradazione del peptide.
Selezionare tra un formato iniettabile o uno spray nasale di frag 176-191 dipenderà dalla natura del disegno dello studio. Se la massima biodisponibilità è importante, l’utilizzo di frag 176-191 iniettabile sarà la scelta migliore. Tuttavia, se la scarsa adesione del soggetto alle iniezioni è una preoccupazione, allora potrebbe valere la pena considerare il formato spray nasale di frag 176-191.
References
Wu, Z., & Ng, F. M. (1993). Antilipogenic action of synthetic C-terminal sequence 177-191 of human growth hormone. Biochemistry and molecular biology international, 30(1), 187–196.
Natera, S. H., Jiang, W. J., & Ng, F. M. (1994). Reduction of cumulative body weight gain and adipose tissue mass in obese mice: response to chronic treatment with synthetic hGH 177-191 peptide. Biochemistry and molecular biology international, 33(5), 1011–1021.
Strobl, J. S., & Thomas, M. J. (1994). Human growth hormone. Pharmacological reviews, 46(1), 1–34.
Vijayakumar, A., Novosyadlyy, R., Wu, Y., Yakar, S., & LeRoith, D. (2010). Biological effects of growth hormone on carbohydrate and lipid metabolism. Growth hormone & IGF research : official journal of the Growth Hormone Research Society and the International IGF Research Society, 20(1), 1–7. https://doi.org/10.1016/j.ghir.2009.09.002
Stier, H., Vos, E., & Kenley, D. (2013). Safety and Tolerability of the Hexadecapeptide AOD9604 in Humans. Journal Of Endocrinology And Metabolism, 3(1-2), 7-15.
Ng, F., Natera, S., Jiang, W.-J. US Patent No. 5,869,452 (1999).
Heffernan, M., Summers, R. J., Thorburn, A., Ogru, E., Gianello, R., Jiang, W. J., & Ng, F. M. (2001). The effects of human GH and its lipolytic fragment (AOD9604) on lipid metabolism following chronic treatment in obese mice and beta(3)-AR knock-out mice. Endocrinology, 142(12), 5182–5189. https://doi.org/10.1210/endo.142.12.8522
Ogru, E., Wilson, J. C., Heffernan, M., Jiang, W. J., Chalmers, D. K., Libinaki, R., & Ng, F. (2000). The conformational and biological analysis of a cyclic anti-obesity peptide from the C-terminal domain of human growth hormone. The journal of peptide research : official journal of the American Peptide Society, 56(6), 388–397. https://doi.org/10.1034/j.1399-3011.2000.00771.x
Berneis, K., & Keller, U. (1996). Metabolic actions of growth hormone: direct and indirect. Bailliere’s clinical endocrinology and metabolism, 10(3), 337–352. https://doi.org/10.1016/s0950-351x(96)80470-8
Cara J. F. (1993). Growth hormone in adolescence. Normal and abnormal. Endocrinology and metabolism clinics of North America, 22(3), 533–552.
Barkan, A. L., Stred, S. E., Reno, K., Markovs, M., Hopwood, N. J., Kelch, R. P., & Beitins, I. Z. (1989). Increased growth hormone pulse frequency in acromegaly. The Journal of clinical endocrinology and metabolism, 69(6), 1225–1233. https://doi.org/10.1210/jcem-69-6-1225
Sharma, R., Luong, Q., Sharma, V. M., Harberson, M., Harper, B., Colborn, A., Berryman, D. E., Jessen, N., Jørgensen, J. O. L., Kopchick, J. J., Puri, V., & Lee, K. Y. (2018). Growth hormone controls lipolysis by regulation of FSP27 expression. The Journal of endocrinology, 239(3), 289–301. https://doi.org/10.1530/JOE-18-0282
Ng, F. M., Jiang, W. J., Gianello, R., Pitt, S., & Roupas, P. (2000). Molecular and cellular actions of a structural domain of human growth hormone (AOD9401) on lipid metabolism in Zucker fatty rats. Journal of molecular endocrinology, 25(3), 287–298. https://doi.org/10.1677/jme.0.0250287
Reed, M. L., Merriam, G. R., & Kargi, A. Y. (2013). Adult growth hormone deficiency – benefits, side effects, and risks of growth hormone replacement. Frontiers in endocrinology, 4, 64. https://doi.org/10.3389/fendo.2013.00064
Heffernan, M. A., Thorburn, A. W., Fam, B., Summers, R., Conway-Campbell, B., Waters, M. J., & Ng, F. M. (2001). Increase of fat oxidation and weight loss in obese mice caused by chronic treatment with human growth hormone or a modified C-terminal fragment. International journal of obesity and related metabolic disorders : journal of the International Association for the Study of Obesity, 25(10), 1442–1449. https://doi.org/10.1038/sj.ijo.0801740
Kwon, D. R., & Park, G. Y. (2015). Effect of Intra-articular Injection of AOD9604 with or without Hyaluronic Acid in Rabbit Osteoarthritis Model. Annals of clinical and laboratory science, 45(4), 426–432.
Ng, F. M., Sun, J., Sharma, L., Libinaka, R., Jiang, W. J., & Gianello, R. (2000). Metabolic studies of a synthetic lipolytic domain (AOD9604) of human growth hormone. Hormone research, 53(6), 274–278. https://doi.org/10.1159/000053183
Ng, F., Jiang, W.-J. International Patent No. WO 99/12969 (1999).
Valentino, M. A., Lin, J. E., & Waldman, S. A. (2010). Central and peripheral molecular targets for antiobesity pharmacotherapy. Clinical pharmacology and therapeutics, 87(6), 652–662. https://doi.org/10.1038/clpt.2010.57
The prohibited list [Internet]. World Anti Doping Agency. 2023 [cited 2023Feb8]. Available from: https://www.wada-ama.org/en/prohibited-list?q=ipamorelin
The UFC Prohibited List [Internet]. USADA. 2023 [cited 2023Feb8]. Available from: https://ufc.usada.org/wp-content/uploads/2023-UFC-Prohibited-List.pdf
Costantino, H. R., Illum, L., Brandt, G., Johnson, P. H., & Quay, S. C. (2007). Intranasal delivery: physicochemical and therapeutic aspects. International journal of pharmaceutics, 337(1-2), 1–24. https://doi.org/10.1016/j.ijpharm.2007.03.025
Alabsi, W., Eedara, B. B., Encinas-Basurto, D., Polt, R., & Mansour, H. M. (2022). Nose-to-Brain Delivery of Therapeutic Peptides as Nasal Aerosols. Pharmaceutics, 14(9), 1870. https://doi.org/10.3390/pharmaceutics14091870