Mi permetto di tradurre e riportare alla attenzione del lettore questo interessante articolo :
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5642081/
L’ormone della crescita (GH) è importante per la promozione della crescita somatica e la regolazione del metabolismo del substrato. L’azione metabolica del GH si verifica in più tessuti tra cui fegato, muscoli, grasso e pancreas, direttamente o indirettamente attraverso il fattore di crescita insulino-simile 1. L’azione diabetogena del GH è stata ben descritta in precedenti studi in vivo. In questo documento, esaminiamo gli effetti metabolici del GH sui tessuti periferici concentrandoci sul metabolismo del glucosio e sull’insulino-resistenza e discutiamo i risultati di studi sull’uomo sugli effetti a lungo termine della somministrazione di GH sull’insulino-resistenza e sull’iperglicemia.
Parole chiave: Ormone della crescita, Glucosio, Metabolismo, Insulino-resistenza
introduzione
L’equilibrio glicemico in circolo è strettamente mantenuto entro il range normale dalla regolazione dinamica sia della produzione di glucosio (dal fegato e dai reni) sia dell’utilizzo del glucosio da parte dei tessuti periferici inclusi fegato, muscoli, grasso e reni .]. L’insulina, il principale regolatore dell’equilibrio del glucosio, abbassa il glucosio plasmatico postprandiale aumentando l’assorbimento e l’utilizzo del glucosio dai tessuti periferici e diminuendo la gluconeogenesi (sintesi di glucosio da precursori non carboidratici come lattato e alanina) e la glicogenolisi (scomposizione del glicogeno in glucosio). Al contrario, gli ormoni controregolatori contro l’azione dell’insulina, come il glucagone e l’epinefrina, prevengono l’ipoglicemia aumentando la gluconeogenesi e la glicogenolisi e diminuendo l’assorbimento e il consumo di glucosio dai tessuti periferici durante il digiuno. L’ormone della crescita (GH) è stato stabilito come uno degli ormoni controregolatori, sin da quando Houssay et al.2 ]. L’effetto diabetogeno del GH è stato supportato anche dall’elevata prevalenza di diabete nei pazienti con acromegalia [ 1 ]. Gli effetti del GH sul controllo glicemico sistemico sono complessi in parte a causa dei suoi effetti indiretti attraverso il fattore di crescita insulino-simile 1 (IGF-1), che ha effetti ipoglicemizzanti simili all’insulina. Ad esempio, gli adulti con deficit di GH sono paradossalmente associati all’obesità addominale e all’insulino-resistenza, che possono essere in parte associati alla loro ridotta azione dell’IGF-1. Questa recensione riassumerà gli effetti diretti e indiretti del GH sul metabolismo del glucosio nei tessuti periferici a livello molecolare e discuterà anche i risultati di studi sull’uomo che studiano l’effetto della somministrazione di GH sul controllo glicemico e sulla resistenza all’insulina.
Effetti del GH sul metabolismo del glucosio
Studi che studiano gli effetti del GH sul metabolismo del glucosio hanno dimostrato che il GH aumenta la produzione di glucosio attraverso la gluconeogenesi e la glicogenolisi dal fegato e dai reni. I pazienti con acromegalia e gli individui umani esposti ad alte dosi di GH hanno mostrato un marcato aumento dell’attività della gluconeogenesi nel fegato e nei reni [ 3 ]. Inoltre, un recente studio in vivo ha dimostrato che il trattamento con GH ha aumentato l’espressione dell’mRNA di 2 principali geni gluconeogenici, la fosfoenolpiruvato carbossi-chinasi e la glucosio-6-fosfatasi, negli epatociti di topo [ 4 ]. È stato riscontrato che la somministrazione di GH aumenta la glicogenolisi negli adulti sani e, inversamente, la microchirurgia ipofisaria nei pazienti con acromegalia riduce la glicogenolisi [ 5] .]. Nonostante l’aumentata glicogenolisi, nei ratti transgenici che sovraesprimono il gene umano del GH è stato riportato un aumento significativo del contenuto di glicogeno epatico , suggerendo un aumento della sintesi di glicogeno dovuto a un eccesso di GH [ 6 ]. Una maggiore attività di glicogeno sintasi è stata riportata anche in quei ratti transgenici GH umani [ 6 ].
Precedenti studi hanno dimostrato che il GH sopprime l’assorbimento del glucosio nel tessuto adiposo. Uno studio in vivo ha dimostrato che la somministrazione di GH nei ratti sopprime la quantità di trasportatore del glucosio 1 (GLUT1) e GLUT4 nella membrana plasmatica degli adipociti [ 7]. Recentemente è stato rivelato il meccanismo molecolare dell’effetto inibitorio del GH sulla traslocazione del GLUT. La risposta cellulare insulino-dipendente, che include il traffico di GLUT4 alla membrana plasmatica, richiede l’attivazione della fosfoinositide 3-chinasi (PI3K), un mediatore chiave della segnalazione metabolica a valle del recettore dell’insulina. La segnalazione PI3K è regolata negativamente dalla subunità regolatoria p85. È stato scoperto che il GH induce l’up-regulation di p85 nei tessuti adiposi bianchi nei topi con produzione eccessiva di GH e negli adipociti trattati con GH in uno studio in vitro [ 8 ]. Questi risultati implicano un meccanismo che coinvolge la resistenza all’insulina indotta da GH attraverso l’up-regolazione della subunità regolatoria p85 di PI3K.
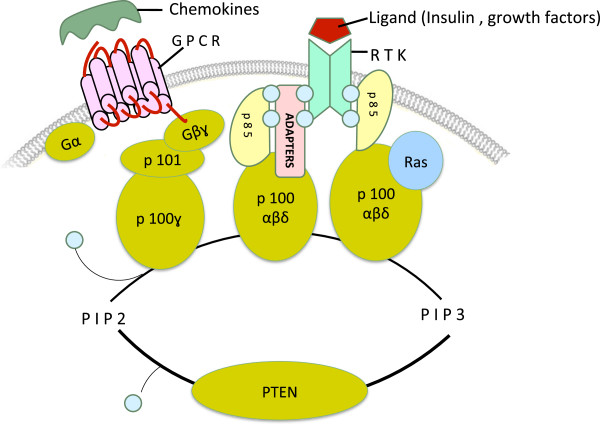
Il GH stimola la lipolisi attraverso l’attivazione della lipasi sensibile agli ormoni, principalmente nel tessuto adiposo viscerale, che si traduce in un flusso di acidi grassi liberi (FFA) dal tessuto adiposo alla circolazione [1 ] . Precedenti studi hanno dimostrato che un aumento di FFA in circolo può indurre insulino-resistenza mediante l’inibizione dell’attività del substrato-1 del recettore dell’insulina (IRS-1) e il conseguente fallimento dell’attivazione di PI3K nel muscolo scheletrico e nel fegato.]. Nel frattempo, l’aumento dell’assorbimento di FFA da parte degli epatociti determina la promozione dell’ossidazione dei lipidi epatici e l’accumulo di acetil coenzima A (acetil-CoA). L’acetil-CoA stimola due enzimi chiave per la gluconeogenesi (piruvato carbossilasi e fosfoenolpiruvato carbossichinasi) e un enzima libera glucosio-6-fosfato sotto forma di glucosio dal fegato e dai reni immettendolo in circolo (glucosio-6-fosfatasi), con conseguente aumento dei livelli di glucosio nel sangue [ 9 ].
Contrariamente agli effetti del GH sul tessuto adiposo, il GH promuove l’assorbimento cellulare di FFA nel muscolo scheletrico aumentando l’attività della lipoproteina lipasi [ 10 ]. La riesterificazione dei trigliceridi da FFA provoca l’accumulo di intermedi lipidici come diacilglicerolo e ceramidi nel muscolo scheletrico [ 11 ]. Precedenti studi hanno rivelato che il diacilglicerolo e la ceramide ostacolano le vie di segnalazione dell’insulina. Il diacilglicerolo attiva la proteina chinasi C theta, che inibisce l’IRS-1 attraverso la fosforilazione della serina, e la ceramide inibisce l’Akt/proteina chinasi B, un importante mediatore della via di segnalazione dell’insulina [11] .]. Come nel tessuto adiposo, l’up-regulation della subunità regolatoria p85 nel muscolo scheletrico da parte del GH era coinvolta nella resistenza all’insulina nei topi con produzione eccessiva di GH [ 12 ].
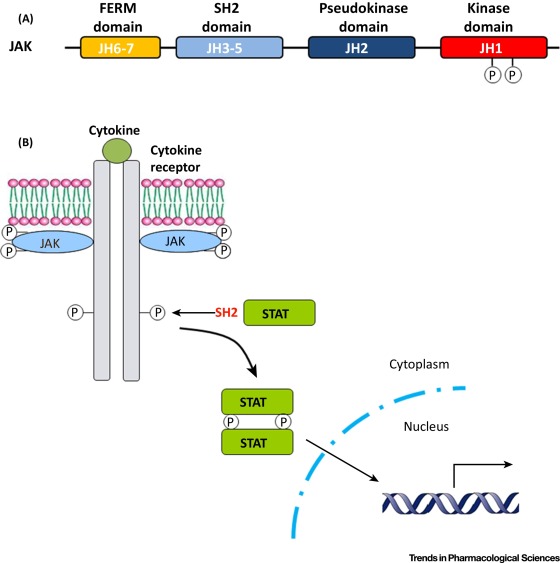
Il cross-talk tra insulina e GH a valle dell’attivazione del recettore nel muscolo scheletrico e nel tessuto adiposo fornisce un altro potente meccanismo alternativo che media la resistenza all’insulina indotta dal GH, supportato da esperimenti sia in vitro che in modelli animali . La produzione di IGF-1 e la crescita somatica da parte del GH è mediata dal trasduttore di segnale Janus chinasi 2 (JAK2) e dall’attivatore della via di segnalazione della trascrizione 5 (STAT5). L’attivazione di STAT5 indotta da GH aumenta l’espressione del soppressore della segnalazione di citochine (SOCS), che interferisce con JAK2/STAT5 e di conseguenza sottoregola l’azione di GH [ 13]. Il crosstalk tra GH e recettori dell’insulina avviene a livello delle proteine SOCS. È stato riportato che la sovraespressione delle proteine SOCS induce insulino-resistenza tramite l’inibizione della fosforilazione dell’IRS-1 indotta dall’insulina o tramite la degradazione dell’IRS-1 [ 14 ]. Nonostante numerosi studi in vitro e modelli animali a sostegno di questa ipotesi, gli studi sull’uomo non sono riusciti a dimostrare gli effetti inibitori diretti del GH sulle vie di segnalazione dell’insulina nel muscolo scheletrico o nel grasso [ 15 ].
L’iperinsulinismo dopo la somministrazione di GH o in condizioni di eccesso di GH sono stati spiegati dalla compensazione delle cellule beta per l’insulino-resistenza; tuttavia, uno studio recente ha scoperto che il GH promuove direttamente la proliferazione delle cellule beta e la secrezione di insulina stimolata dal glucosio [ 16 ]. In teoria, FFA persistentemente elevati in eccesso cronico di GH (ad es. acromegalia) possono causare l’apoptosi delle cellule beta e una conseguente diminuzione della secrezione di insulina [ 17 ], ma l’evidenza in vivo non è chiara.
Effetti dell’IGF-1 sul metabolismo del glucosio
L’eccessiva somministrazione di GH o GH in vivo è seguita da un aumento dei livelli circolanti di IGF-1, pertanto gli effetti netti del GH sul metabolismo del glucosio sono complicati dagli effetti dell’IGF-1. I recettori per l’IGF-1 e l’insulina sono altamente omologhi nella struttura e nella funzione biologica. Il legame dei ligandi provoca l’autofosforilazione dei domini chinasi intracellulari e la successiva attivazione delle cascate di segnalazione a valle, che regolano la trascrizione genica coinvolta nel metabolismo del substrato, nella crescita cellulare e nella differenziazione. L’IGF-1 e l’insulina attivano fortemente i rispettivi recettori, ma possono anche legarsi e attivare debolmente i reciproci recettori [ 18 ]. IGF-1 aveva causato un effetto ipoglicemizzante in precedenti in vivostudi attraverso la stimolazione dell’assorbimento del glucosio e della gluconeogenesi, possibilmente tramite l’attivazione dell’IGF-1 o tramite i recettori dell’insulina [ 19 ]. Ad esempio, la somministrazione di IGF-1 umano ricombinante a topi con deficit del recettore dell’insulina ha indotto effetti insulino-mimetici, tra cui sia un aumento dell’assorbimento di glucosio da parte del muscolo scheletrico sia una diminuzione della gluconeogenesi epatica, attraverso l’attivazione del recettore dell’IGF-1. Coerentemente con questo, l’infusione di IGF-1 ha migliorato i livelli di glucosio nel siero in individui con diabete mellito [ 20 ].
Trattamento con GH e metabolismo del glucosio negli adulti con deficit di GH
Le presentazioni cliniche degli adulti con deficit di GH sono caratterizzate da un aumento dell’adiposità viscerale, dell’insulino-resistenza, della dislipidemia e dell’iperglicemia, che contribuiscono ad aumentare il rischio di morbilità e mortalità cardiovascolare [2 ] . Poiché l’IGF-1 ha proprietà antinfiammatorie ed è importante per l’assorbimento del glucosio dai tessuti periferici, i disturbi metabolici negli adulti con deficit di GH possono essere spiegati dal deficit di IGF-1 [1 ] . Una privazione della lipolisi indotta da GH e il conseguente aumento dell’adiposità viscerale sono anche coinvolti nell’aumento degli FFA circolanti e dell’insulino-resistenza in questi pazienti [ 2 ]. È stato riportato che la maggior parte dei disturbi metabolici, tra cui adiposità viscerale, sarcopenia, ipertensione e dislipidemia, sono alleviati dopo il trattamento con GH.1 ]. Tuttavia, una serie di studi ha suggerito che ci sono possibili impatti negativi sull’omeostasi del glucosio come una ridotta tolleranza al glucosio e sensibilità all’insulina nei pazienti con carenza di GH dopo la somministrazione di GH. In particolare, l’interpretazione degli studi sull’uomo relativi al trattamento con GH e ai cambiamenti associati del metabolismo del glucosio è complessa, poiché il dosaggio e la durata del GH, nonché l’età, l’indice di massa corporea (BMI) e la storia familiare di diabete nei partecipanti allo studio possono influenzare i risultati dello studio .
Il dosaggio originale del trattamento con GH utilizzato negli adulti con deficit di GH era un dosaggio elevato adattato al peso corporeo derivato dal dosaggio utilizzato nei bambini con deficit di GH, tuttavia questa pratica è cambiata in un dosaggio individualizzato con dosi più basse per evitare eventi avversi di trattamento eccessivo dall’inizio degli anni 2000. Molti dei primi studi che utilizzavano dosi elevate di GH (≥0,01 mg/kg/die) riportavano che i livelli di glucosio e insulina a digiuno aumentavano dopo un trattamento a breve termine con GH per meno di 6 mesi, ma di solito venivano ripristinati ai livelli basali dopo 1 o 2 anni del trattamento con GH (Tabella 1). Il trattamento con GH ad alte dosi è risultato efficace per la riduzione della massa grassa totale e viscerale [ 21 , 22 ]. Tuttavia, la sostituzione a lungo termine del GH ad alte dosi ha ridotto la sensibilità all’insulina e ha aggravato la resistenza all’insulina, che può essere spiegata dagli effetti anti-insulina del GH. Nonostante l’aumentata insulino-resistenza, i livelli di emoglobina A1c ( HbA1c ) sono rimasti invariati sia nel trattamento a breve che a lungo termine.Tabella 1).
Tabella 1.
Effetti del trattamento con GH umano ricombinante sul metabolismo del glucosio negli adulti con deficit di GH
| Studio | Numero di casi di GHD | Età (anni) | Dose giornaliera di GH | Durata del GHT | Risultati |
|---|---|---|---|---|---|
| Dose elevata | |||||
| Fowelin et al. [35] | 9 | 38–63 | 0,023mg/kg | 6 settimane | ↑glicemia a digiuno, ↑insulina, ↓IS (EC) |
| 26 settimane | ↔Glucosio a digiuno, ↔insulina, ↓IS (EC) | ||||
| Chipman et al. [36] | AO (rhGH=52, P=46) | 43.5±9.8 | 0,012mg/kg | 6 mesi | ↑Glucosio a digiuno, ↔insulina, ↔HbA1c |
| 18 mesi | ↔Glucosio a digiuno, ↔insulina, ↔HbA1c | ||||
| CO (rhGH=32, P=35) | 28.4±7.2 | 0,012mg/kg | 6 mesi | ↑Glucosio a digiuno, ↑insulina, ↔HbA1c | |
| 18 mesi | ↔Glucosio a digiuno, ↔insulina, ↔HbA1c | ||||
| Hwu et al. [ 21 ] | rhGH=7, P=9 | 20–44 | 0,011mg/kg | 6 mesi | ↔Glucosio a digiuno, ↔IS (MIST) |
| 12 mesi | ↔Glucosio a digiuno, ↓IS (MIST) | ||||
| Cristoforo et al. [ 37 ] | rhGH=7, P=7 | 43.7±4.1 | 0,011mg/kg | 6 mesi | ↑Glucosio a digiuno, ↔insulina, ↔HbA1c |
| 24 mesi | ↔Glucosio a digiuno,↑insulina, ↓IS (EC) | ||||
| Rosenfalk et al. [ 22 ] | 11 | 26–57 | 0,016mg/kg | 30 mesi | ↑AUC glicemia, ↑AUC insulina (OGTT), ↓IS (FSIGT) |
| Sesmilo et al. [38] | rhGH=20, P=20 | 24–64 | 0,01mg/kg | 6 mesi | ↑Glucosio a digiuno,↑insulina, ↔HbA1c |
| 18 mesi | ↑Glucosio a digiuno, ↔insulina, ↔HbA1c | ||||
| Chrisoulidou et al. [39] | rhGH=12, C=21 | 52±10 | 0.7 mg | 7 Years | ↔Fating glucose, ↔insulin, ↔AUC gluc, ↑AUC insulin (OGTT) |
| Giavoli et al. [40] | 20 | 44±14 | 0.01–0.024 mg/kg | 1 Year | ↑Fasting gluose, ↑HOMA-IR, ↓QUICKI |
| 5 Years | ↑Fasting gluose, ↔HOMA-IR, ↔QUICKI | ||||
| Low dose | |||||
| al-Shoumer et al. [41] | 13 | 24–65 | 0.008 mg/kg | 1 Year | ↑Fasting gluose, ↑AUC gluc,↑AUC insulin (OGTT) |
| 4 Years | ↔Fasting glucose, ↔AUC gluc, ↔AUC insulin (OGTT) | ||||
| Gibney et al. [42] | rhGH=10, P=11 | 21–51 | 0.008 mg/kg | 10 Years | ↔Fasting glucose, ↔insulin, ↔c-peptide |
| Svensson et al. [43] | 11 | 52±3.9 | 0.61 mg | 7 Years | ↔Fasting glucose, ↔insulin, ↔IS (EC) |
| Bramnert et al. [44] | rhGH=10, P=9 | 42±2.6 | 0.009 mg/kg | 1 Week | ↑Fasting glucose, ↑insulin, ↓IS (EC) |
| 6 Months | ↑Fasting glucose, ↑insulin, ↓IS (EC) | ||||
| Yuen et al. [25] | 8 | 32–59 | 0.1 mg | 12 Months | ↓Fasting glucose, ↔insulin, ↑HOMA-S |
| 8 | 31–60 | 0.5 mg | ↔Fasting glucose, ↔insulin, ↔HOMA-S | ||
| Roemmler et al. [45] | rhGH=22, C=30 | 27–82 | 0.30 mg | 2–42 Years (mean 11) | ↓Fasting glucose, ↔insulin, ↔HOMA-IR, ↔HbA1c, ↔AUC gluc, ↔AUC insulin, ↔IS (OGTT) |
| Woodmansee et al. [23] | No DM (rhGH=337, C=134) | 48.9±0.7 | 0.36 mg | 2.33±1.34 Years | ↔IFG (>109 mg/dL), ↔HbA1c |
| DM (rhGH=64, C=35) | 56.0±1.7 | ↔IFG (>109 mg/dL), ↔HbA1c | |||
| Elbornsson et al. [24] | 156 | 22-74 | 0.40 mg | 15 Years | ↑Fasting glucose (year 1–year 10), ↓HbA1c (year 7–year 15) |
| Yuen and Dunger [26] | rhGH=8, C=9 | 46±3.7 | 0.005 mg/kg | 3 Months | ↔Fasting glucose, ↔insulin, ↑IS (EC) |
| Weber et al. [46] | 245 | 49±14 | 0,37 mg | 4 anni | ↔Glucosio a digiuno, ↔HbA1c |
L’età del partecipante è stata presentata in media ± deviazione standard o intervallo.
GH, ormone della crescita; GHD, carenza di ormone della crescita; GHT, trattamento dell’ormone della crescita; IS, sensibilità all’insulina; CE, pinza euglicemica; AO, esordio in età adulta; HbA 1c , emoglobina glicosilata; CO, esordio infantile; rhGH, ormone della crescita umano ricombinante; MIST, test di soppressione dell’insulina modificato; HOMA-IR, valutazione del modello di omeostasi dell’insulino-resistenza; AUC gluc, l’area sotto la curva del glucosio; AUC insulina, l’area sotto la curva per l’insulina; OGTT, test di tolleranza al glucosio orale; P, placebo; FSIGT, test di tolleranza al glucosio per via endovenosa a campionamento frequente; QUICKI, indice di controllo quantitativo dell’insulina; HOMA-S, valutazione del modello di omeostasi della sensibilità all’insulina.
È stato riportato che la somministrazione di GH a basse dosi negli adulti con deficit di GH è efficace nel migliorare la composizione corporea, anche se in misura minore rispetto al GH ad alte dosi [ 23 , 24 ]. La maggior parte degli studi che utilizzano il trattamento con GH a basso dosaggio (<0,01 mg/kg/die) non ha dimostrato alcun cambiamento significativo o solo un aumento transitorio dei livelli di glucosio a digiuno (Tabella 1). La maggior parte di questi studi ha riportato resistenza all’insulina e sensibilità all’insulina invariate dopo il trattamento a lungo termine con GH a basso dosaggio. Due studi condotti dagli stessi ricercatori [ 25 , 26 ] hanno mostrato un miglioramento della sensibilità all’insulina nei pazienti obesi con deficit di GH dopo un trattamento a breve termine con una dose fissa di GH a basso dosaggio (0,1 mg/die). La maggior parte degli studi con trattamento con GH a basso dosaggio non ha riportato cambiamenti significativi nei livelli di HbA1c , sebbene alcuni studi abbiano mostrato una lieve diminuzione dell’HbA1c entro il range normale negli adulti con deficit di GH [ 24 ]. Uno studio ha studiato l’effetto del GH sui livelli di glucosio a digiuno e sull’HbA1cin pazienti con deficit di GH con diabete mellito preesistente, e ha rivelato un lieve aumento della glicemia a digiuno senza significatività statistica e nessun peggioramento dei valori di HbA1c [ 23 ] .
Recenti studi hanno valutato il rischio di sviluppo di diabete mellito dopo trattamento con basse dosi di GH (Tavolo 2). Poiché gli adulti con deficit di GH sono a maggior rischio di ridotta tolleranza al glucosio rispetto alla popolazione generale, è sufficiente confrontare l’incidenza del diabete nei pazienti trattati con GH con quella dei pazienti non trattati. Attualmente, solo uno studio di durata relativamente breve (2,3 anni) ha riportato che non vi era alcun aumento del rischio di diabete mellito negli adulti con deficit di GH dopo il trattamento con GH rispetto ai controlli con deficit di GH non trattati [27 ] . Altri studi hanno confrontato l’incidenza del diabete tra i pazienti trattati con GH e la popolazione generale normale, e la maggior parte di essi non ha rivelato un aumento significativo dell’incidenza del diabete dopo 2-10 anni di trattamento con GH.Tavolo 2). Uno studio ha dimostrato un’incidenza di diabete mellito da 2 a 6 volte superiore a quella prevista nella popolazione generale normale [ 28 ]. È interessante notare che in questo studio l’aumento dell’età e del BMI, il sesso femminile e la durata del GH, ma non la dose di GH, sono stati associati ad un aumentato rischio di diabete mellito [ 28 ] .
Tavolo 2.
Effetti del trattamento con GH umano ricombinante sullo sviluppo di DM negli adulti
| Studio | Numero di casi | Età (anni) | Dose giornaliera di GH | Durata del GHT | Risultati |
|---|---|---|---|---|---|
| Attanasio et al. [47] | 2.922 negli Stati Uniti, 3.709 in Europa | 45.4±15 | – | 4,1 anni | ↔prevalenza DM (11,3% negli Stati Uniti, 5,7% in Europa) |
| ↔Incidenza di DM (n/1.000 anni-paziente: 14,1 negli Stati Uniti, 7,0 in Europa) | |||||
| Lüger et al. [ 28 ] | 5.143 coorte KIMS | 49±13 | 0,36 mg | 3,9 anni | ↑Incidenza di DM 26/1.000 anni-paziente |
| Hartmann et al. [ 27 ] | rhGH=1.988, controllo=442 | 46±15 | <0,012 mg/kg | 2,3 anni | ↔incidenza di DM |
| Shimatsu et al.[ 48 ] | 209 in Giappone | 18–64 | 0,25 mg | 2 anni | ↔incidenza di DM |
L’età del partecipante è stata presentata in media ± deviazione standard o intervallo.
GH, ormone della crescita; DM, diabete mellito; GHT, trattamento dell’ormone della crescita; KIMS, database metabolico internazionale Pfizer; rhGH, ormone della crescita umano ricombinante.
Trattamento di GH e metabolismo del glucosio in bambini e adolescenti con deficit di GH
Ad oggi, sono stati condotti relativamente pochi studi che esaminano il cambiamento del metabolismo del glucosio dopo il trattamento con GH nella popolazione pediatrica. La maggior parte di questi studi ha dimostrato che durante la terapia con GH in bambini e adolescenti con deficit di GH è stato osservato un aumento dell’insulino-resistenza, indicato da un aumento dell’insulina a digiuno e dalla valutazione del modello di omeostasi dei livelli di insulino-resistenza, ma i loro livelli di glucosio a digiuno/postprandiale e di HbA1c sono rimasti entro intervallo normale (Tabella 3). Un numero limitato di studi sul clamp euglicemico ha riportato una diminuzione della sensibilità all’insulina nei bambini con deficit di GH dopo un trattamento a breve termine con GH [ 29 , 30 ].
Tabella 3.
Effetti del trattamento con GH umano ricombinante sul metabolismo del glucosio in bambini e adolescenti con deficit di GH
| Studio | Numero di casi | Età (anni) | Dose giornaliera di GH | Durata del GHT | Risultati |
|---|---|---|---|---|---|
| Saenger et al. [ 49 ] | GHD=70 | – | 0,05mg/kg | 5 anni | ↔Glucosio a digiuno/postprandiale, ↑insulina a digiuno/postprandiale, ↔HbA1c |
| Heptulla et al. [ 29 ] | GHD=6, ISS=2 | 12±1 | 0,05mg/kg | 6 mesi | ↔Glucosio a digiuno, ↑insulina, ↓IS (HC) |
| Radetti et al. [ 50 ] | GHD=128, controllo sano=40 | 8.9±3.2 | 0,04-0,05 mg/kg | 6 anni | ↓QUICK, nessun caso con IGT, DM a 6 anni |
| Salerno et al. [51] | GHD=30, controllo sano=30 | 9.3±0.5 | 0,03mg/kg | 2 anni | ↔glicemia a digiuno, ↑insulina, ↑HOMA-IR |
| Metwalley et al. [52] | GHD=30, controllo sano=20 | 4–10 | 1 mg/ m2 | 1 anno | ↑glicemia a digiuno, ↑insulina, ↑HOMA-IR |
| Meazza et al. [53] | GHD=16, controllo sano=20 | 3.4–14.7 | 0,025mg/kg | 1 anno | ↑glicemia a digiuno, ↑insulina |
| Ramistella et al. [54] | GHD=32, controllo sano=33 | 8.9±3.6 | 0,03mg/kg | 2 anni | ↔glicemia a digiuno, ↑insulina, ↑HOMA-IR |
| Ciresi et al. [ 30 ] | GHD=73, controllo sano=50 | 10.3±2.8 | 0,025-0,033 mg/kg | 1 anno | ↔Glucosio a digiuno, ↔insulina, ↑HOMA-IR, ↓QUICKI, ↔AUC glic, ↓AUC insulina (OGTT),↓IS (HC) |
L’età del partecipante è stata presentata in media ± deviazione standard o intervallo.
GH, ormone della crescita; GHT, trattamento dell’ormone della crescita; GHD, carenza di ormone della crescita; HbA 1c , emoglobina glicosilata; IS, sensibilità all’insulina; HC, morsetto iperglicemico; QUICKI, indice di controllo quantitativo dell’insulina; IGT, alterata tolleranza al glucosio; DM, diabete mellito; HOMA-IR, valutazione del modello di omeostasi dell’insulino-resistenza; AUC gluc, l’area sotto la curva del glucosio; AUC insulina, l’area sotto la curva per l’insulina; OGTT, test orale di tolleranza al glucosio.
Poiché l’aumento della resistenza all’insulina e la ridotta sensibilità all’insulina sono collegati al rischio di intolleranza al glucosio e diabete mellito, sono state sollevate preoccupazioni in merito al possibile sviluppo di diabete mellito durante o dopo il trattamento con GH a lungo termine.Tabella 4). Con l’avvento della ricerca del National Cooperative Growth Study [ 31 ], ampi studi farmacoepidemiologici hanno dimostrato che l’incidenza del diabete mellito di tipo 2 è aumentata di oltre 6 volte nei bambini sottoposti a trattamento con GH rispetto alla popolazione generale, specialmente nei pazienti con fattori di rischio predisponenti per diabete, come obesità, storia familiare di diabete, sindrome di Turner, sindrome di Prader-Will o trattamento con glucocorticoidi [ 32 , 33 ]. Lo sviluppo del diabete mellito non era associato alla dose o alla durata del trattamento con GH e l’incidenza del diabete mellito di tipo 1 durante il trattamento con GH era paragonabile a quella della popolazione generale in tutti e tre gli studi [ 31-33]. In confronto, un recente studio francese basato sulla popolazione ha riportato che la prevalenza del diabete mellito nei bambini trattati con GH era simile alla popolazione generale quando i pazienti raggiungevano la prima età adulta [ 34 ]. Da notare che questo studio ha incluso pazienti con deficit isolato di GH, bassa statura idiopatica o bambini bassi nati piccoli per l’età gestazionale, escludendo i pazienti con alto rischio di mortalità e morbilità, come i pazienti con cancro, insufficienza renale cronica, ormone ipofisario multiplo deficit, sindrome di Turner o sindrome di Prader-Willi [ 34 ].
Tabella 4.
Effetti del trattamento con GH umano ricombinante sullo sviluppo del DM nei bambini e negli adolescenti
| Studio | Numero di casi | Età (anni) | Dose giornaliera di GH | Durata del GHT | Risultati |
|---|---|---|---|---|---|
| Bleten et al. [ 31 ] | >19.000 coorte NCGS | 7.2–12.9 (all’iscrizione) | – | – | ↑Incidenza di DM in soggetti con fattori di rischio identificabili |
| Cutfield et al. [ 32 ] | 23.333 coorte KIGS | 10.3 (7.2–12.7) | 0,03 mg / kg (0,02-0,04) | 2,9 anni | ↑incidenza di T2DM in soggetti con fattori di rischio identificabili, ↔incidenza di T1DM |
| Bambino et al. [ 33 ] | 11.686 coorte GeNeSIS | 10.2 (6.5–12.7) | 0,04 mg / kg (0,03-0,05) | 2,5 anni | ↑incidenza di T2DM in soggetti con fattori di rischio identificabili, ↔incidenza di T1DM |
| Poidvin et al. [34] | 5,100 French SAGhE cohort (iGHD, ISS, SGA) | 20–44 | 0,03±0,01mg/kg | 4 anni | ↔prevalenza DM |
L’età del partecipante è stata presentata in media ± deviazione standard, mediana (intervallo interquartile) o intervallo.
GH, ormone della crescita; DM, diabete mellito; GHT, trattamento dell’ormone della crescita; NCGS, Studio Nazionale sulla Crescita Cooperativa; KIGS, Pharmacia e Upjohn International Growth Study; T1DM, diabete mellito di tipo 1; DMT2, diabete mellito di tipo 2; GeNeSIS, pazienti trattati con GH nel Genetics and Neuroendocrinology of Short Stature International Study; SAGhE, sicurezza e adeguatezza dei trattamenti con ormone della crescita in Europa; iGHD, deficit isolato dell’ormone della crescita; ISS, bassa statura idiopatica; SGA, piccolo per età gestazionale.
Riepilogo
La terapia con GH antagonizza l’azione dell’insulina sui tessuti periferici, come il muscolo scheletrico, il fegato e il tessuto adiposo, aumentando così la produzione di glucosio dal muscolo scheletrico e dal fegato e riducendo l’assorbimento di glucosio dal tessuto adiposo. La produzione di insulina è aumentata per compensare l’aumento del glucosio circolante dopo la somministrazione di GH. La lipolisi indotta da GH nel tessuto adiposo viscerale e il conseguente aumento di FFA circolanti interferiscono anche con le vie di segnalazione dell’insulina e l’esposizione cronica ad alti FFA può esercitare tossicità diretta nelle beta-cellule. Nel frattempo, l’IGF-1 ha azioni insulino-mimetiche nel muscolo scheletrico e nel fegato e l’aumento dell’IGF-1 circolante dopo la somministrazione di GH può avere effetti benefici sull’omeostasi del glucosio e sulla resistenza all’insulina.
Numerosi studi sull’uomo hanno suggerito che la somministrazione di GH negli adulti con deficit di GH può ridurre l’adiposità viscerale e migliorare i disturbi cardio-metabolici. Tuttavia, alcuni studi hanno sollevato preoccupazioni per l’aumento dell’insulino-resistenza e la compromissione della glicemia a digiuno durante il trattamento con GH, specialmente nei pazienti obesi e nei pazienti anziani. Studi su bambini e adolescenti hanno anche suggerito che la somministrazione di GH può indurre insulino-resistenza nel trattamento a breve termine, ma le sue conseguenze a lungo termine non sono state ancora completamente determinate. Studi di coorte internazionali indicano che la terapia con GH può aumentare l’incidenza del diabete mellito di tipo 2 in bambini e adolescenti con fattori di rischio predisponenti, pertanto è prudente monitorare le possibili conseguenze negative sul metabolismo del glucosio durante e dopo la somministrazione di GH.
Riferimenti
1.
Vijayakumar A, Yakar S, Leroith D. L’intricato ruolo dell’ormone della crescita nel metabolismo. Front Endocrinol (Losanna) 2011; 2 :32. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]2.
Moller N, Jorgensen JO. Effetti dell’ormone della crescita sul metabolismo del glucosio, dei lipidi e delle proteine nei soggetti umani. Endocr Rev. 2009; 30 :152–77. [ PubMed ] [ Google Scholar ]3.
Schwarz JM, Mulligan K, Lee J, Lo JC, Wen M, Noor MA, et al. Effetti dell’ormone della crescita umano ricombinante sul metabolismo epatico dei lipidi e dei carboidrati nei pazienti con infezione da HIV con accumulo di grasso. J Clin Endocrinol Metab. 2002; 87 :942. [ PubMed ] [ Google Scholar ]4.
Kim YD, Li T, Ahn SW, Kim DK, Lee JM, Hwang SL, et al. Il piccolo partner eterodimero del recettore nucleare orfano regola negativamente l’induzione mediata dall’ormone della crescita della gluconeogenesi epatica attraverso l’inibizione del trasduttore di segnale e l’attivatore della transattivazione della trascrizione 5 (STAT5). J Biol Chem. 2012; 287 :37098–108. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]5.
Hoybye C, Chandramouli V, Efendic S, Hulting AL, Landau BR, Schumann WC, et al. Contributo della gluconeogenesi e della glicogenolisi alla produzione epatica di glucosio nell’acromegalia prima e dopo la microchirurgia ipofisaria. Ricerca Horm Metab. 2008; 40 :498–501. [ PubMed ] [ Google Scholar ]6.
Cho Y, Ariga M, Uchijima Y, Kimura K, Rho JY, Furuhata Y, et al. I nuovi ruoli del fegato per la compensazione dell’insulino-resistenza nei ratti transgenici dell’ormone della crescita umano. Endocrinologia. 2006; 147 :5374–84. [ PubMed ] [ Google Scholar7.
Kilgour E, Baldwin SA, Flint DJ. Regolazione divergente dei trasportatori di glucosio GLUT1 e GLUT4 degli adipociti di ratto da parte di GH. J Endocrinolo. 1995; 145 :27–33. [ PubMed ] [ Google Scholar ]8.
del Rincon JP, Iida K, Gaylinn BD, McCurdy CE, Leitner JW, Barbour LA, et al. Regolazione dell’ormone della crescita dell’espressione di p85alfa e dell’attività della fosfoinositide 3-chinasi nel tessuto adiposo: meccanismo per la resistenza all’insulina mediata dall’ormone della crescita. Diabete. 2007; 56 : 1638–46. [ PubMed ] [ Google Scholar ]9.
Kovacs P, Stumvoll M. Acidi grassi e resistenza all’insulina nei muscoli e nel fegato. Best Pract Res Clin Endocrinol Metab. 2005; 19 :625-35. [ PubMed ] [ Google Scholar ]10.
LeRoith D, Yakar S. Meccanismi della malattia: effetti metabolici dell’ormone della crescita e del fattore di crescita simile all’insulina 1. Nat Clin Pract Endocrinol Metab. 2007; 3 :302–10. [ PubMed ] [ Google Scholar ]11.
Coen PM, Goodpaster BH. Ruolo dei lipidi intramiocellulari nella salute umana. Tendenze Endocrinol Metab. 2012; 23 :391–8. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]12.
Barbour LA, Shao J, Qiao L, Leitner W, Anderson M, Friedman JE, et al. L’ormone della crescita placentare umano aumenta l’espressione dell’unità regolatoria p85 della fosfatidilinositolo 3-chinasi e innesca una grave insulino-resistenza nel muscolo scheletrico. Endocrinologia. 2004; 145 :1144–50. [ PubMed ] [ Google Scholar ]13.
Ram PA, Waxman DJ. Inibizione della proteina SOCS/CIS della segnalazione STAT5 stimolata dall’ormone della crescita mediante molteplici meccanismi. J Biol Chem. 1999; 274 :35553–61. [ PubMed ] [ Google Scholar ]14.
Rui L, Yuan M, Frantz D, Shoelson S, White MF. SOCS-1 e SOCS-3 bloccano la segnalazione dell’insulina mediante degradazione mediata dall’ubiquitina di IRS1 e IRS2. J Biol Chem. 2002; 277 :42394–8. [ PubMed ] [ Google Scholar ]15.
Krusenstjerna-Hafstrom T, Madsen M, Vendelbo MH, Pedersen SB, Christiansen JS, Moller N, et al. Segnalazione di insulina e GH nel muscolo scheletrico umano in vivo in seguito all’esposizione esogena di GH: impatto di un carico di glucosio orale. PLoS One. 2011; 6 :e19392. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]16.
Wu Y, Liu C, Sun H, Vijayakumar A, Giglou PR, Qiao R, et al. Il recettore dell’ormone della crescita regola l’iperplasia delle cellule beta e la secrezione di insulina stimolata dal glucosio nei topi obesi. J Clin Invest. 2011; 121 :2422–6. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]17.
Unger RH, Zhou YT. Lipotossicità delle cellule beta nell’obesità e in altre cause di spillover di acidi grassi. Diabete. 2001; 50 Supplemento 1 :S118–21. [ PubMed ] [ Google Scholar ]18.
Boucher J, Tseng YH, Kahn CR. I recettori dell’insulina e del fattore di crescita simile all’insulina-1 agiscono come modulatori di ampiezza specifici del ligando di un percorso comune che regola la trascrizione genica. J Biol Chem. 2010; 285 :17235–45. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]19.
Mauras N, Haymond MW. Gli effetti metabolici di GH e IGF-I sono separabili? Crescita Horm IGF Res. 2005; 15 :19–27. [ PubMed ] [ Google Scholar ]20.
Moses AC, Young SC, Morrow LA, O’Brien M, Clemmons DR. Il fattore di crescita insulino-simile umano I ricombinante aumenta la sensibilità all’insulina e migliora il controllo glicemico nel diabete di tipo II. Diabete. 1996; 45 :91–100. [ PubMed ] [ Google Scholar ]21.
Hwu CM, Kwok CF, Lai TY, Shih KC, Lee TS, Hsiao LC, et al. La sostituzione dell’ormone della crescita (GH) riduce il grasso corporeo totale e normalizza la sensibilità all’insulina negli adulti con deficit di GH: un rapporto sull’esperienza clinica di un anno. J Clin Endocrinol Metab. 1997; 82 :3285–92. [ PubMed ] [ Google Scholar ]22.
Rosenfalck AM, Maghsoudi S, Fisker S, Jorgensen JO, Christiansen JS, Hilsted J, et al. L’effetto di 30 mesi di terapia sostitutiva a basso dosaggio con ormone della crescita umano ricombinante (rhGH) sulla cinetica dell’insulina e del peptide C, sulla secrezione di insulina, sulla sensibilità all’insulina, sull’efficacia del glucosio e sulla composizione corporea negli adulti con deficit di GH. J Clin Endocrinol Metab. 2000; 85 :4173–81. [ PubMed ] [ Google Scholar ]23.
Woodmansee WW, Hartman ML, Lamberts SW, Zagar AJ, Clemmons DR, International Hypo CCSAB. Presenza di glicemia a digiuno alterata negli adulti con deficit di GH che ricevono la sostituzione di GH rispetto ai soggetti non trattati. Clin Endocrinol (Oxf) 2010; 72 :59–69. [ PubMed ] [ Google Scholar ]24.
Elbornsson M, Gotherstrom G, Bosaeus I, Bengtsson BA, Johannsson G, Svensson J. Quindici anni di sostituzione con GH migliorano la composizione corporea e i fattori di rischio cardiovascolare. Eur J Endocrinolo. 2013; 168 :745–53. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]25.
Yuen KC, Dunger DB. Effetti persistenti sui livelli di glucosio a digiuno e sulla sensibilità all’insulina dopo 6 mesi di interruzione di una terapia con GH a dosi molto basse negli adulti con grave deficit di GH. Clin Endocrinol (Oxf) 2006; 64 :549–55. [ PubMed ] [ Google Scholar ]26.
Yuen KC, Roberts CT, Jr, Frystyk J, Rooney WD, Pollaro JR, Klopfenstein BJ, et al. La terapia a breve termine con GH a basse dosi migliora la sensibilità all’insulina senza modificare il metabolismo del cortisolo e l’accumulo di grasso ectopico negli adulti con deficit di GH. J Clin Endocrinol Metab. 2014; 99 :E1862–9. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]27.
Hartman ML, Xu R, Crowe BJ, Robison LL, Erfurth EM, Kleinberg DL, et al. Sorveglianza prospettica della sicurezza degli adulti con deficit di GH: confronto tra pazienti trattati con GH e pazienti non trattati. J Clin Endocrinol Metab. 2013; 98 :980–8. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]28.
Luger A, Mattsson AF, Koltowska-Haggstrom M, Thunander M, Goth M, Verhelst J, et al. Incidenza del diabete mellito ed evoluzione dei parametri glicemici nei soggetti con deficit dell’ormone della crescita durante la terapia sostitutiva dell’ormone della crescita: uno studio osservazionale a lungo termine. Cura del diabete. 2012; 35 :57–62. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]29.
Heptulla RA, Boulware SD, Caprio S, Silver D, Sherwin RS, Tamborlane WV. Diminuzione della sensibilità all’insulina e iperinsulinemia compensatoria dopo il trattamento ormonale nei bambini con bassa statura. J Clin Endocrinol Metab. 1997; 82 :3234–8. [ PubMed ] [ Google Scholar ]30.
Ciresi A, Ciccio F, Amato MC, Giordano C. Rivalutazione del comportamento clinico e metabolico dei bambini con deficit isolato dell’ormone della crescita durante il trattamento con GH secondo la nuova nota 39 dell’Agenzia Italiana del Farmaco (AIFA) J Endocrinol Invest . 2015; 38 :1301–7. [ PubMed ] [ Google Scholar ]31.
Blethen SL, Allen DB, Graves D, August G, Moshang T, Rosenfeld R. Sicurezza dell’ormone della crescita derivato dall’acido desossiribonucleico ricombinante: l’esperienza del National Cooperative Growth Study. J Clin Endocrinol Metab. 1996; 81 :1704–10. [ PubMed ] [ Google Scholar ]32.
Cutfield WS, Wilton P, Bennmarker H, Albertsson-Wikland K, Chatelain P, Ranke MB, et al. Incidenza del diabete mellito e ridotta tolleranza al glucosio nei bambini e negli adolescenti sottoposti a trattamento con ormone della crescita. Lancetta. 2000; 355 :610–3. [ PubMed ] [ Google Scholar ]33.
Child CJ, Zimmermann AG, Scott RS, Cutler GB, Jr, Battelino T, Blum WF, et al. Prevalenza e incidenza del diabete mellito nei bambini e negli adolescenti trattati con GH: analisi dal programma di ricerca osservazionale GeNeSIS. J Clin Endocrinol Metab. 2011; 96 :E1025–34. [ PubMed ] [ Google Scholar ]34.
Poidvin A, Weill A, Ecosse E, Coste J, Carel JC. Rischio di diabete trattato nella prima età adulta dopo il trattamento con ormone della crescita della bassa statura durante l’infanzia. J Clin Endocrinol Metab. 2017; 102 :1291–8. [ PubMed ] [ Google Scholar ]35.
Fowelin J, Attvall S, Lager I, Bengtsson BA. Effetti del trattamento con ormone della crescita umano ricombinante sulla sensibilità all’insulina e sul metabolismo del glucosio negli adulti con deficit dell’ormone della crescita. Metabolismo. 1993; 42 :1443–7. [ PubMed ] [ Google Scholar ]36.
Chipman JJ, Attanasio AF, Birkett MA, Bates PC, Webb S, Lamberts SW. Il profilo di sicurezza della terapia sostitutiva con GH negli adulti. Clin Endocrinol (Oxf) 1997; 46 :473–81. [ PubMed ] [ Google Scholar ]37.
Christopher M, Hew FL, Oakley M, Rantzau C, Alford F. I difetti dell’azione dell’insulina e del metabolismo del glucosio nei muscoli scheletrici negli adulti con deficit di ormone della crescita persistono dopo 24 mesi di terapia con ormone della crescita umano ricombinante. J Clin Endocrinol Metab. 1998; 83 :1668–81. [ PubMed ] [ Google Scholar ]38.
Sesmilo G, Biller BM, Llevadot J, Hayden D, Hanson G, Rifai N, et al. Effetti della somministrazione dell’ormone della crescita su marcatori di rischio infiammatorio e cardiovascolare negli uomini con deficit dell’ormone della crescita. Uno studio clinico randomizzato e controllato. Ann Intern Med. 2000; 133 :111–22. [ PubMed ] [ Google Scholar ]39.
Chrisoulidou A, Beshyah SA, Rutherford O, Spinks TJ, Mayet J, Kyd P, et al. Effetti di 7 anni di terapia sostitutiva dell’ormone della crescita negli adulti ipopituitari. J Clin Endocrinol Metab. 2000; 85 :3762–9. [ PubMed ] [ Google Scholar ]40.
Giavoli C, Porretti S, Ronchi CL, Cappiello V, Ferrante E, Orsi E, et al. Monitoraggio a lungo termine della sensibilità all’insulina negli adulti con deficit di ormone della crescita in terapia sostitutiva con ormone della crescita umano ricombinante. Metabolismo. 2004; 53 :740–3. [ PubMed ] [ Google Scholar ]41.
al-Shoumer KA, Gray R, Anyaoku V, Hughes C, Beshyah S, Richmond W, et al. Effetti del trattamento di quattro anni con l’ormone della crescita umano biosintetico (GH) sull’omeostasi del glucosio, sulla secrezione di insulina e sul metabolismo dei lipidi negli adulti con deficit di GH. Clin Endocrinol (Oxf) 1998; 48 :795-802. [ PubMed ] [ Google Scholar ]42.
Gibney J, Wallace JD, Spinks T, Schnorr L, Ranicar A, Cuneo RC, et al. Gli effetti di 10 anni di ormone della crescita umano ricombinante (GH) in pazienti adulti con deficit di GH. J Clin Endocrinol Metab. 1999; 84 :2596–602. [ PubMed ] [ Google Scholar ]43.
Svensson J, Fowelin J, Landin K, Bengtsson BA, Johansson JO. Effetti di sette anni di terapia sostitutiva con GH sulla sensibilità all’insulina negli adulti con deficit di GH. J Clin Endocrinol Metab. 2002; 87 :2121–7. [ PubMed ] [ Google Scholar ]44.
Bramnert M, Segerlantz M, Laurila E, Daugaard JR, Manhem P, Groop L. La terapia sostitutiva dell’ormone della crescita induce la resistenza all’insulina attivando il ciclo degli acidi grassi del glucosio. J Clin Endocrinol Metab. 2003; 88 :1455–63. [ PubMed ] [ Google Scholar ]45.
Roemmler J, Kuenkler M, Schneider HJ, Dieterle C, Schopohl J. Confronto del metabolismo del glucosio e dei lipidi e della mineralizzazione ossea in pazienti con deficit dell’ormone della crescita con e senza sostituzione a lungo termine dell’ormone della crescita. Metabolismo. 2010; 59 :350–8. [ PubMed ] [ Google Scholar ]46.
Weber MM, Biller BM, Pedersen BT, Pournara E, Christiansen JS, Hoybye C. L’effetto della sostituzione dell’ormone della crescita (GH) sull’omeostasi del glucosio nel sangue in pazienti adulti non diabetici con deficit di GH: dati reali dal NordiNet(R ) Studio sui risultati internazionali. Clin Endocrinol (Oxf) 2017; 86 :192–8. [ PubMed ] [ Google Scholar ]47.
Attanasio AF, Jung H, Mo D, Chanson P, Bouillon R, Ho KK, et al. Prevalenza e incidenza del diabete mellito nei pazienti adulti sottoposti a sostituzione dell’ormone della crescita per deficit dell’ormone della crescita: un’analisi del database di sorveglianza. J Clin Endocrinol Metab. 2011; 96 :2255–61. [ PubMed ] [ Google Scholar ]48.
Shimatsu A, Tai S, Imori M, Ihara K, Taketsuna M, Funai J, et al. Efficacia e sicurezza della terapia sostitutiva dell’ormone della crescita negli adulti giapponesi con deficit dell’ormone della crescita: uno studio osservazionale post-marketing. Endocr J. 2013; 60 :1131–44. [ PubMed ] [ Google Scholar ]49.
Saenger P, Attie KM, DiMartino-Nardi J, Fine RN. Metabolismo dei carboidrati nei bambini che ricevono l’ormone della crescita per 5 anni. Insufficienza renale cronica confrontata con deficit dell’ormone della crescita, sindrome di Turner e bassa statura idiopatica. Gruppo di collaborazione Genentech. Pediatric Nephrol. 1996; 10 :261–3. [ PubMed ] [ Google Scholar ]50.
Radetti G, Pasquino B, Gottardi E, Contadin IB, Rigon F, Aimaretti G. Sensibilità all’insulina nei bambini con deficit di ormone della crescita: influenza del trattamento sostitutivo. Clin Endocrinol (Oxf) 2004; 61 :473–7. [ PubMed ] [ Google Scholar ]51.
Salerno M, Esposito V, Farina V, Radetti G, Umbaldo A, Capalbo D, et al. Miglioramento delle prestazioni cardiache e dei fattori di rischio cardiovascolare nei bambini con deficit di GH dopo due anni di terapia sostitutiva con GH: uno studio osservazionale, aperto, prospettico, caso-controllo. J Clin Endocrinol Metab. 2006; 91 :1288–95. [ PubMed ] [ Google Scholar ]52.
Metwalley KA, Farghaly HS, Abd El-Hafeez HA. Valutazione della massa e della funzione del ventricolo sinistro, del profilo lipidico e dell’insulino-resistenza nei bambini egiziani con deficit dell’ormone della crescita: uno studio prospettico caso-controllo a centro singolo. Indian J Endocrinol Metab. 2013; 17 :876–82. [ Articolo gratuito PMC ] [ PubMed ] [ Google Scholar ]53.
Meazza C, Elsedfy HH, Pagani S, Bozzola E, El Kholy M, Bozzola M. Parametri metabolici e profilo adipochinico nei bambini con deficit di ormone della crescita (GHD) prima e dopo il trattamento con GH di 12 mesi. Ricerca Horm Metab. 2014; 46 :219–23. [ PubMed ] [ Google Scholar ]54.
Ramistella V, Wasniewska M, Arasi S, Catena M, Velletri MR, Corica D, et al. Studio trasversale e prospettico degli effetti della terapia con GH sul pannello metabolico nei bambini con deficit di GH. Pediatric Med Chir. 2014; 36 :104. [ PubMed ] [ Google Scholar ]